オルガノイドとは何か?オルガノイドとスフェロイドの違いは?
オルガノイドという言葉を聞く機会が増えてきました。
初めて耳にしたのは実験医学2017年10月号。
2回目は2018年に参加した再生医療学会でした。
大会場にもかかわらず立ち見の人が会場を埋め尽くし、移動するのも大変なほど。武部先生のプレゼンでした。
オルガノイドとは一体どんな概念なのか?
スフェロイドとオルガノイドの違いは何なのか?
今回はこの2点に焦点をあてます。
目次
オルガノイドとは?

出典:Stemcell.com
オルガノイドとは、わかりやすく言うと、
詳しくは、
生体内の組織・器官を、本物の組織・器官にそっくりな構造・機能で、体の外(in vitro)で観察したり使用したりできるので、
医薬品候補の早期絞り込み、毒性試験、疾患の病態研究、高齢者・小児など脆弱集団を対象とした複数薬剤併用時の安全性の研究、さらには直接移植による治療にまで応用が広がっています。
オルガノイドは、多能性幹細胞(ES細胞、iPS細胞)やがん細胞から創出されます。その形成過程は、初期発生と同様に、自己凝集反応や自己組織化をたどります。
オルガノイドで何が可能になるのか?
オルガノイドについて最初に理解しようとしたとき、
「オルガノイドは一体何か?」にフォーカスしたのですが、当時はあまり理解できませんでした。
オルガノイドは何か?よりも、
オルガノイドで一体何が可能になるのか?
と考えたところ、オルガノイドについてイメージしやすくなりました。
オルガノイドは器官別に、
脳オルガノイド、肝オルガノイド、腸オルガノイド、腎オルガノイドと呼ばれます。

出典:Modeling mouse and human development using organoid cultures
たとえば、腸オルガノイドの中には、蠕動様運動を自律的に行い、医薬品などの成分を吸収・分泌する能力を持つものがあります。このような腸オルガノイドを利用することで、ヒトを対象とせずに、in vitroで医薬品の腸管での吸収や代謝を評価することが可能となります。
毒性試験、疾患研究、創薬研究などにおいて必須とされていた動物実験を実施しなくてもよくなる可能性があります。
また、腸オルガノイド、肝オルガノイドについては、移植により治療に応用するための研究も行われています。
ドナー臓器の不足を解決する手段としても注目されています。
オルガノイドとスフェロイドの違い
オルガノイドについて大体のイメージを持つことができました。
すると、こんな疑問がわいてきます。
次はこれについてみていきます。
スフェロイドについてより詳しく知りたい場合
オルガノイド、スフェロイドなどの三次元培養と、二次元培養についてぶどうにイメージを借りるとわかりやすくなりました。
ぶどうには、黄緑色や紫色、赤紫色のものがありますよね。1房のぶどうにはたくさんのぶどうの粒がついています。
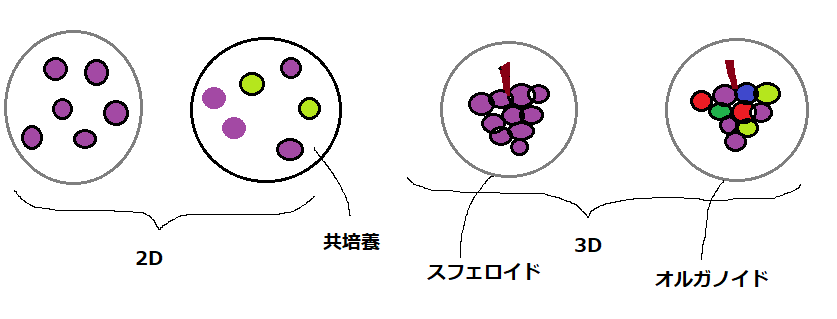
お皿にブドウの粒を置いた状態、ぶどうの房ごと置いた状態を、培養ディッシュに置き換えて考えてみます。
ぶどうの粒をばらばらに置いた状態が二次元培養。単一色のぶどうの粒のみあるのがシングルセル培養です。複数の色の粒がある状態が共培養です。
ふさになっている状態が三次元培養で、
単一色のつぶが集合して、房を形成した状態がスフェロイドのイメージ、
複数の色の粒からなる房を形成した状態がオルガノイドのイメージです。
さらに、マイクロ流体デバイスを利用して血流や微小環境を模倣し、動的な環境における細胞のふるまいを観察できるようにしたものがオーガン・オン・チップ(Organ-on-a-chip)です。

出典:elveflow.com
もう少し詳しく考えてみると、
スフェロイドは、オルガノイドを形成する途中過程の、発展途上な状態だといえます。
スフェロイドに異種の細胞が加わり、各細胞が細胞選別によって、自身のいるべき場所に移動して、機能を持つ組織体を形成したのがオルガノイドだと考えています。つまり、スフェロイドをより生体に近い状態に近づけたものがオルガノイドです。
オルガノイドの力学モデル
オルガノイドについておおまかに理解できたところで、武部先生の研究グループによる肝オルガノイドについて調べてみました。
そのなかで、
オルガノイドが細胞接着性を示す基板上で形成される現象が興味深かったので、ご紹介します。
粒子の自己組織化に必要な2つの要素
こちらの記事でも細胞の接着性については触れましたが、
培養プレートで、細胞が基板に接着せず、凝集するためには、次の式を満たす必要があります。
Ucell-cell > Ucell-sub
Ucell-cell:細胞-細胞間の接着エネルギー
Ucell-sub:細胞-基板間の接着エネルギー
市販の培養基板は、上記の式を満たすように、細胞と基板との接着強度が最小になるように、つまり細胞非接着性になるように設計されています。
それでは、細胞と基板との接着強度が小さければ小さいほど、細胞同士が凝集しやすくなるのか?というと、そうではないことがわかっています。
分子が凝集し、規則正しく並んだ結晶構造を形成するためには、分子と分子間に適度が引力が必要となります。細胞同士の接着強度が強すぎると、細胞同士が近すぎて、回転などがしにくくなり、適切な場所に配列できなくなります。
適切な接着強度、適切な引力の2つの要素がそろって初めて、細胞が凝集し、結晶化できます。
すると、前述の、オルガノイドが細胞接着性を示す基板上で形成されることは、上記の特徴と矛盾しますよね。
オルガノイド形成に必要な力学的要素
オルガノイドはマトリゲルという生体由来のハイドロゲル基板上で形成されます。
この基板は、前述の通り、細胞接着性を示すものです。
肝オルガノイド創出には、間葉系幹細胞(MSC)が必要です。MSCの分化や運動は、ゲル基板の硬さに影響を受けることがわかっています。
一般に、基板が硬いほど、MSCは基板に接着しやすくなることがわかっています。
すると、基板が柔らかいほど、MSCは凝集しやすくなるはずです。
実際は、中間の硬さのときに、最も効率よく凝集体が形成されることがわかっています。
このことより、ゲル基板の硬さが、細胞-基板間だけでなく、細胞-細胞間の相互作用にも影響を与えることがわかり、最適なオルガノイド創出のためには、硬さを適切に設定したゲル基板が必要であることが報告されています。
オルガノイドの基板が細胞接着性なのは、細胞が接着を介して基板の硬さを認識し、基板の硬さが細胞-基板間と、細胞-細胞間の相互作用を制御している、ということなのですね。
まとめ
漠然と耳にしていたオルガノイドは、創薬研究の重要なツールだけでなく、再生医療・組織工学にも関係することがわかりました。
武部先生のグループは、肝芽オルガノイドをマウスに移植したところ、48~72時間以内に血液灌流が生じたことを報告しています。
今回はオルガノイドについて一部を紹介しました。今後は、肝オルガノイド、がんオルガノイド、腸オルガノイドなどの研究動向もチェックしていきます。
【参考】
日本再生医療学会雑誌Vol.17 Issue03
※アイキャッチ画像の出典:Stemcell.com