代謝特性により未分化幹細胞を除去/高精度に心筋細胞を精製する方法とは?【心臓再生医療】
予後が極めて悪いとされる末期重症心不全の唯一の根本的治療法は心臓移植です。
しかし、ドナー不足のため、待期期間中に亡くなる方は少なくありません。
心臓移植治療に替わるものとして、心臓再生医療が注目されています。今回ご紹介する技術を知ったときには、本当に驚きました。
大量培養が難しいと言われている心筋細胞を、高純度で、安価な方法で、大量に精製できる日は遠くないかもしれません。胸が高鳴る技術です。
慶応大学の遠山周吾先生・福田恵一先生が確立された手法が臨床応用されれば、心臓再生医療における最大の問題、「量」と「質」を克服できる可能性があります。
目次
未分化幹細胞を除去/高精度に心筋細胞を精製する方法
iPS細胞から心筋細胞を分化誘導する場合、100%が心筋細胞になるわけではありません。
最も効率が良い場合:90%が心筋細胞になる
最も効率が悪い場合:30%が心筋細胞になる
つまり、最も効率よく分化誘導できたとしても、他の細胞が10%残存していることになります。
iPS細胞は夢の技術と言われますが、細胞移植で使うためには、移植する細胞に他の細胞が残存することは避けなければなりません。
このように、
必要または不要な細胞を分離する技術が、再生医療の分野では強く求められています。
再生医療をさらに本格化するためには、次の分離技術が必要です。
・高精度
・非侵襲的
・大量分離が可能
これまでレーザや刺激応答性ポリマーを用いて不要細胞を除去する手法などが開発されています。
近年は、このような細胞外部からのアプローチではなく、細胞の代謝の違いを利用して細胞を分離する技術が開発されています。
心筋細胞の代謝の特性を利用した細胞分離技術
この技術は簡単に言うと、
心筋細胞と非心筋細胞の代謝の違いを利用して、
不要な非心筋細胞だけを死滅させる方法です。
つまり、
心筋細胞のみが生き残れて、心筋細胞以外の細胞は生き残れない培養環境をつくりだしたのです。
ここで、心筋細胞以外には、心筋細胞以外の細胞や、未分化の幹細胞が含まれます。
あまり良い例えではありませんが、
水の中でないと生きられない魚を陸に挙げて、人だけが生き残れるようにしたイメージですね。
心筋細胞と多能性幹細胞の代謝の違い
心筋細胞と多能性幹細胞の代謝を比較したところ、
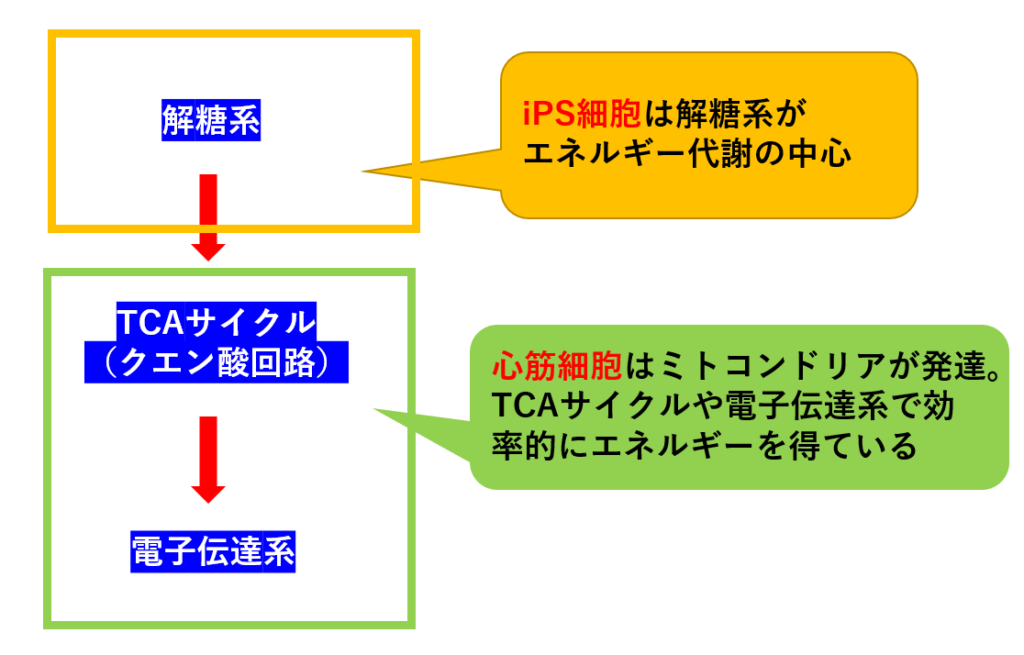
iPS細胞やES細胞などの幹細胞は、十分な酸素がある環境においても、解糖系がエネルギー代謝の中心になっていることがわかりました。
解糖系が中心ということは、グルコースを大量に利用しています。
一方で、
心筋細胞は、ミトコンドリアが発達しており、TCAサイクル(クエン酸回路)や電子伝達系を利用してエネルギーを得ていることがわかりました。
それをもう少し詳しく書いたのがこちら。
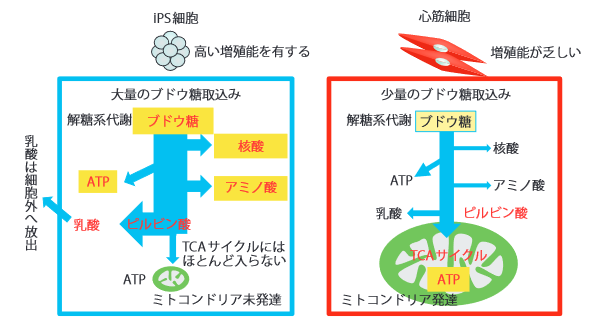
出典:iPS細胞を用いた循環器領域の再生医療
iPS細胞はグルコースを大量に取り込んで、解糖系で拡散、アミノ酸、乳酸を合成します。TCAサイクルへはほとんど入りません。
一方、心筋細胞は、少量のグルコースを解糖系を介してTCAサイクルへ送り、TCAサイクルで効率的にエネルギーを得ています。
では、心筋細胞だけが生き残れる環境を作るためにはどうすればいいでしょうか?
iPS細胞が増殖に必要とする、グルコースを全く含まない培地を用意させればいいわけですよね。

ただ、グルコースをカットすると、心筋細胞もエネルギーを得られなくなりますので、心筋細胞が増殖するのに必要な乳酸を添加しました。
グルコースを除去し、乳酸のみを添加した「無グルコース乳酸添加培地」でマウスES細胞や、肝細胞、腎細胞、リンパ球を培養したところ、いずれの細胞もすみやかに死滅しました。
一方で、ラット由来の心筋細胞は無グルコース乳酸添加で生存率が著しく上昇することを認めました。

出典:iPS細胞を用いた循環器領域の再生医療
この技術で得られる心筋細胞の純化度は99.5%以上になったようです。
遠藤先生方の報告によると、残る0.5%にも未分化幹細胞は検出されておらず、免疫不全マウスに移植しても奇形腫などの形成は認めていません。
細胞毎の代謝特性を利用して、培地の組成を変えるだけという単純なやり方なのがすごいですよね。
これだけでも十分な精度だと思いますが、2017年の日本薬理学会誌では、さらに高純度に精製する手法が報告されています。
グルタミンを除去してさらに純化度を上げる培地を開発
遠藤先生方の研究によると、多能性幹細胞はグルコースの代謝だけでなく、グルタミンの代謝にも依存することがわかりました。
つまり、グルコースを除去するだけではまだ足りないということです。
多能性幹細胞の生存において、グルコースの非存在下では、グルタミンの代謝が活性化され、これによりATP合成されていることがわかりました。
出典:ヒトのES細胞およびiPS細胞の生存におけるグルタミンの代謝の役割を改変
ということは、グルコースを除去するだけでなく、グルタミンも除去することで、未分化細胞の残存率を下げられることになります。
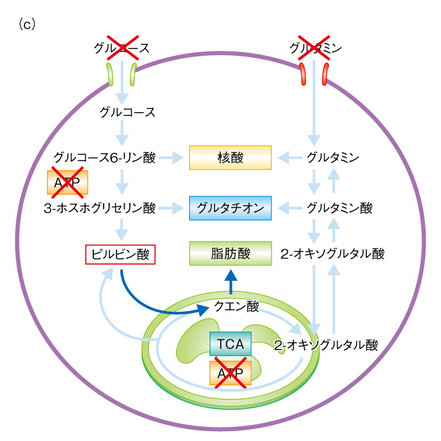
簡単に、グルタミン代謝に依存しているメカニズムを補足しておきます。
ポイントは、TCAサイクルに登場するアコニターゼとイソクエン酸デヒドロゲナーゼです。

出典:wikipediaを改変
図で青い★のついた箇所のアコニターゼとイソクエン酸デヒドロゲナーゼ。多能性幹細胞は、この2つの発現が低いのが特徴です。
そのため、TCAサイクル後半に進むことができません。TCAサイクル後半に進むために、多能性幹細胞はグルタミンを利用して、α-ケトグルタル酸(2-オキソグルタル酸)を得ています。
グルタミン酸をなくしてしまえば、どうがんばってもTCAサイクル後半に進めません。
このように、グルコース非存在下で、最後の頼みの綱であるグルタミンも除去すれば、未分化の多能性幹細胞はもう生き残るすべがありません。

出典:ヒトのES細胞およびiPS細胞の生存におけるグルタミンの代謝の役割を改変
※2-オキソグルタル酸=α-ケトグルタル酸(混乱しがちなので補足しておきます)
このようにして開発された、無グルコース無グルタミン乳酸添加培地を利用することで、心筋細胞の純化精製効率がさらに向上されました。
この手法は、低コストかつ単純ですので、再生医療への応用が期待されますね。
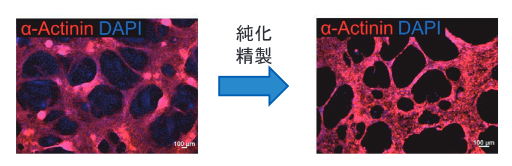
出典:日薬理誌(Folia Pharmacol.Jpn.)150,246~250(2017)
それで、どこまで開発が進んでいるか気になりますよね。
2016年までのものしか入手できていないのですが、平成28年度委託研究開発成果報告書によると、
無グルコース無グルタミン乳酸添加培地を利用したiPS細胞由来の心筋細胞を用いて、心筋梗塞モデルのマイクロミニブタへの移植実験がすでに行われています。
iPS細胞由来の心筋細胞を移植した群では、MRIで左室駆出率の有意な改善を認めています。
臨床試験に向かって進んでいるようですね。しかも、残存する未分化iPS細胞は、0.001%以下だったとのこと。すごいですよね。
この技術、最新動向がすごく気になります。次回再生医療学会で報告があるはずです。今年はいけませんでしたので、来年は絶対行きます。
【参考】
ES細胞あるいはiPS細胞に由来する心筋細胞の代謝の特性を利用した大量精製法の確立
代謝的アプローチによる ES および iPS 細胞における未分化幹細胞除去法および心筋精製法
ヒトのES細胞およびiPS細胞の生存におけるグルタミンの代謝の役割
※アイキャッチ画像の出典:ヒトのES細胞およびiPS細胞の生存におけるグルタミンの代謝の役割
こちらの記事もおすすめ
mRNA医薬という新しい治療戦略-実用化の鍵を握るDDSキャリアとは?