【ネイチャー論文を解説】移植後に長期生存が可能な免疫不全ブタモデルの作製に成功(慶応大・佐賀大の快挙)

どんなに評判の良いレストランが目と鼻の先にあったとしても、そこへ行くまでの橋がなかったらレストランにはたどり着けませんよね。

橋があるからそのレストランへ行けるように、
再生医療においても、開発した人工臓器をヒトで臨床応用するためには、動物で安全性や有効性を確認する必要があります。
適切な動物モデルがなければ、せっかく開発した人工臓器を実用化できないのです。その橋渡しとなる動物モデルの作製に成功したことが、慶応大と佐賀大より発表されました。
今回の研究は、研究成果を非臨床試験から臨床試験に橋渡しする画期的な成果だと言えます。
主役はブタです。今回は2019年5月21日付けでネイチャーに掲載された以下の論文を深掘りします。
目次
人工臓器の臨床応用における障壁突破につながる本研究のポイント
バイオプリンタでヒト細胞由来の人工血管を作製しても、ヒトにより近い大きな動物で有効性や安全性を確認できなければ、ヒトを対象とする臨床試験へ進むことができません。
適切な動物モデルがないことは、人工臓器を臨床応用するうえで障壁となります。
マウスやラットなどの小さな動物では、ヒトに使用する大きな臓器を評価するのに大きさが足りないのです。
そこで、実験動物としてブタモデルの開発が行われてきましたが、免疫不全状態にしたブタモデルには長期間生存が難しいという課題がありました。
今回の研究のすごいところは、ヒトの組織を移植しても、長期間生存できるブタモデルを作製し、その安全性・有効性を確認したことです。
本研究のポイント
長期生存が可能な、免疫不全ブタモデルの作製に成功した
バイオ3Dプリンタで作製した人工血管の有効性・安全性をブタで確認した
従来の課題
人工血管などの人工臓器をヒト以外の動物に移植する場合(異種移植といいます)、動物にとって人工臓器は異物になります。そのため、人工臓器が拒絶されないように、動物の免疫機能を抑える必要があります。
しかし、数ヵ月にわたって免疫抑制することは容易でなく、遺伝子操作で免疫不全にしたブタの場合、長期間生存するのが難しいという問題がありました。
本研究の解決方法
これまでは、免疫抑制剤を使用したり、遺伝子操作によってブタを免疫不全状態にしていました。
慶応大・佐賀大の研究では、免疫抑制剤の使用に加え、免疫の主役臓器である脾臓と胸腺を摘出しています。
| 従来 | 今回 |
| 免疫抑制剤や遺伝子操作 | ・胸腺と脾臓を摘出
・免疫抑制剤を使用 |
「免疫抑制剤を使用したブタ」、「免疫抑制剤+脾臓・胸腺を摘出したブタ」それぞれの頸動脈静脈にバイパス移植を行い、移植した人工血管の生着の具合や、血管壁の厚さ、血管の開存度を比較しました。
結果
両者で大きな違いが確認されました。
| 免疫抑制剤を使用したブタ(対照)n=6 | 免疫抑制剤+脾臓・胸腺を摘出したブタ n=6 |
| 2週間以内に血管は閉塞 | すべてのブタで開存を確認 |
具体的には、免疫抑制剤+脾臓・胸腺を摘出したブタでは、
移植してから、
2週間後に2頭から人工血管を摘出、
1ヵ月後に2頭から人工血管を摘出、
3ヵ月後に2頭から人工血管を摘出し、各時点での開存度や閉塞の有無を確認しています。
すべてのタイミングで、開存は維持され、閉塞を認めませんでした。内径は拡大し、縦方向へも伸長していることが確認され、血管壁も3ヵ月かけて徐々に厚くなっていることが確認されました。
これに対し対照群では、すべてのブタで血栓の形成により、2週間以内の閉塞を認めました。
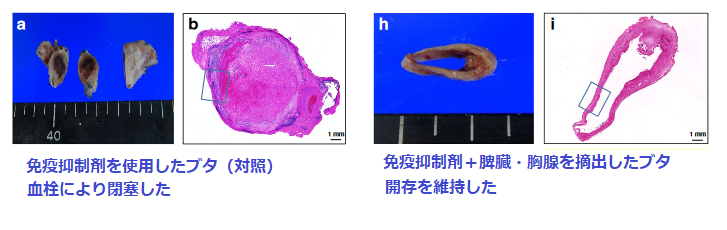
Development of an immunodeficient pig modelallowing long-term accommodation of artificialhuman vascular tubesから引用、追記
また、対照群に比べ、免疫抑制剤+脾臓・胸腺を摘出したブタでは、リンパ球浸潤が劇的に抑えられていることがわかります。
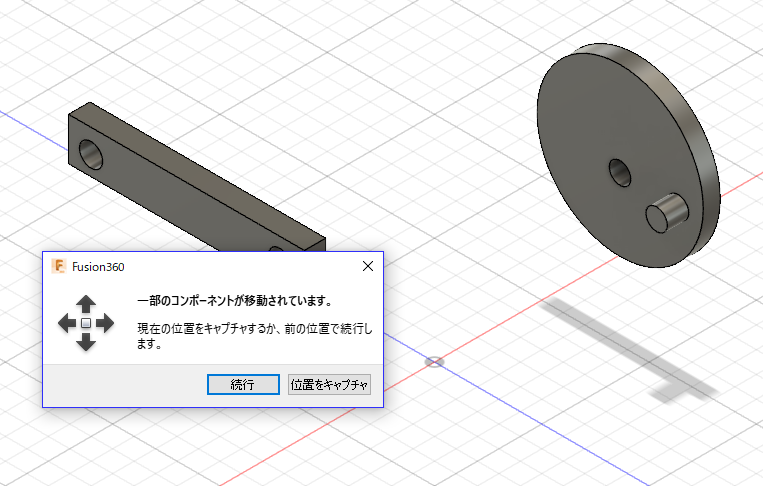
Development of an immunodeficient pig modelallowing long-term accommodation of artificialhuman vascular tubesから引用、追記
この結果より、免疫抑制剤に加えて胸腺・脾臓を摘出したブタモデルでは、免疫反応が抑制され、血管は開存を維持しながら伸長し、厚くなっていったことがわかります。
論文によると、対照群(免疫抑制剤のみを使用)での血管肥厚は、急激な免疫反応であるのに対し、胸腺・脾臓を摘出したブタモデルで徐々に血管壁が厚くなったのは、圧力と体積の負荷によるものだろうとされています。本来の自然な反応によって血管壁が厚くなったということでしょうか。
「免疫抑制剤+脾臓・胸腺を摘出したブタ」の優れたところ
従来の免疫不全ブタモデルと比較して、本研究の免疫不全ブタモデルは次の2点でさらに優れています。
・SPF環境下で飼育しなくてもよい
・免疫抑制剤の用量を調整することで、成熟ブタにも適用可能である
SPF(Specific Pathogen Free)というのは、実験の結果に影響を及ぼしうる病原菌がいないことが保証された条件を指します。つまり、厳格に管理された飼育環境です。
本研究で作製されたブタモデルは、SPF環境下で飼育しなくても免疫反応や感染をコントロールできたとされています。SPF環境の維持には莫大なコストがかかりますので、SPF環境が不要であることは、大きな利点といえます。
また、今回の研究ではミニブタを使用していますが、免疫抑制剤の用量を調整することで、成熟ブタモデルにも同様の手法が適用できるとされています。
本研究の特筆すべきところ
本研究による「初」のポイントとして、次の一文があります。
tissue-engineered grafts derived from human cells remained patent for> 1 month after xenotransplantation in a large animal model.
組織工学的に作製されたヒト細胞由来グラフトを大きな動物モデルに異種移植後、1ヵ月を超えて開存を維持した
これに対し、免疫抑制剤のみで処置したブタモデルでは、2週間経たずに閉塞と炎症細胞浸潤を認めています。
長期生存が難しいと言われていた大きな免疫不全ブタモデルで、人工血管が1ヵ月以上にわたり開存を維持したことから、
ヒトにより近い動物で、
人工臓器の安全性・有効性の検証が長期間可能になったわけですね。
非臨床試験におけるブタの使用促進につながる研究成果になりそうですね。
ちなみに、慶応大のプレスリリースでは移植した人工血管の開存と血管組織の再生を最長20週確認した、とありますが、20週については論文では確認できませんでした。他の論文に記載のある情報かもしれません(あるいは私の見落としか・・・)。
まとめ
ネイチャーの論文には記載されていませんが、今回使用されたバイオプリンタはサイフューズ社と澁谷工業が開発したレジェノバであることは間違いないと思います。
過去記事でもご紹介しましたが、レジェノバで作製される人工血管は、外来物質からなるスキャフォールドを使用せず、ヒト由来細胞の自家細胞を使用したものです。
小林英司先生、中山功一先生、伊藤学先生方の最終目標は、臨床応用であることが論文に記載されています。これに関するものとして、先月、透析用血管にレジェノバで作製した患者の皮膚由来人工血管を移植する臨床試験が申請されましたね。
今回の研究成果が、臨床試験承認の後押しになるのは間違いないと思います。
再生医療で人工臓器を作製しても、それを評価する手段が十分でなかったり、今回のように臨床試験開始までこぎつけるための動物実験の実施に壁が存在したりしていますね。
バイオプリンティングの技術にばかり目がいっていましたが、どんなにすごい人工臓器を開発しても、それを臨床応用につなげられなければ、治療を待っている人への解決手段にはなりませんよね。
今回の研究は、研究成果を非臨床試験から臨床試験に橋渡しする画期的な成果だと言えます。
今後の動向が気になりますね。最新情報が入りましたらまたシェアさせていただきます。
※アイキャッチ画像の出典:nature.com
【参考】