レトロウイルスをわかりやすく解説|仕組みから内在性レトロウイルスをめぐる再生医療まで

生物は遺伝情報という大事な情報をDNAという箱に保存しています。
遺伝情報を使いたい時は、DNAの情報をRNAという箱に一旦移して、目的のもの(タンパク質)を作っています。

つまり、生物にとって
DNAは遺伝情報を保存するためのもの
RNAは遺伝情報を利用するためのもの
なんですね。
ウイルスの場合、生物と違い、遺伝情報をDNA、RNAのどちらかに保存しています。
ウイルスができるのは、遺伝情報を保存することだけで、遺伝情報を自分で利用することはできません。

ウイルスが遺伝情報を利用するためには、宿主細胞に侵入し、宿主細胞のシステムを利用しなければなりません。
遺伝情報をRNAに保存しているウイルスをRNAウイルス、
遺伝情報をDNAに保存しているウイルスをDNAウイルスといいます。
今回は数多くあるRNAウイルスのうち、レトロウイルスに注目します。
目次
レトロウイルスを簡単に言うと
RNAウイルスには、自分のコピーを増やすために、DNAにならないタイプとDNAになるタイプがあります。
RNAを鋳型として相補的なRNAを合成して、宿主の翻訳機構を利用して増えていくタイプがDNAにならないタイプ、
RNAから一度DNAを合成して、宿主の翻訳機構を利用して増えていくタイプがDNAになるタイプで、
レトロウイルスは後者に属します。

レトロウイルスの構造

レトロウイルスは上図のように、RNAがタンパク質のカプシドで包まれ、それが脂質二重層からなるエンベロープで囲まれた構造になっています。
レトロウイルスの生活環

出典:sciencewindow.jst.go.jp
レトロウイルスが細胞内に侵入すると、一番外側のエンベロープがとれます(①)。
次に、自分の持っているRNAと逆転写酵素を使い、RNAからDNAをつくります(③)。さらにもう1つDNAを合成することで、ウイルスのゲノム情報をもったDNA二本鎖ができあがります(④)。
ウイルスDNAを今度は宿主染色体に組み込みます。これはインテグラーゼという酵素によって行われます(⑤)。
宿主染色体に組み込まれたDNAはプロウイルスと呼ばれます(⑤)。プロウイルスは組み込まれた状態で眠り続けることもあれば、宿主細胞の転写・翻訳機構を利用して、ウイルスタンパク質を合成することもあります。
(エイズの原因となるHIVウイルスもレトロウイルスで、プロウイルスとして潜伏状態を維持できることは薬剤による治療が難しい原因の1つになっています)。
次に、宿主細胞のRNAポリメラーゼによって、ウイルスDNAからたくさんのRNAコピーが生成され、ウイルスの遺伝情報が複製されていきます(⑧)。
レトロトランスポゾンとレトロウイルスの違い
ゲノムの中を動く遺伝子をトランスポゾンといい、過去記事でもご紹介しました。
過去記事:
「動く」という意味では、ウイルスは究極の動く遺伝子といえますよね。遺伝情報を持ち、動き回ることができます。
トランスポゾンの中でも、RNAを中間体としてDNAを合成し、それがDNAの別の部位に挿入されるタイプをレトロトランスポゾンといいました。レトロウイルスもレトロトランスポゾンも、RNAを中間体としてDNAを合成する点は同じですね。
では、レトロトランスポゾンとレトロウイルスの違いはなんでしょうか?
違いは、移動範囲にあります。
レトロトランスポゾンが細胞のDNAの別の場所にしか移動できず、その細胞を離れることができないのに対し、レトロウイルスは宿主細胞を抜け出して別の細胞に入り込むことができます。
レトロトランスポゾンが進化によって移動能力を獲得したのがレトロウイルス、と考えることもできますね。
遺伝子導入への応用「ウイルスベクター」
レトロウイルスはウイルスを増やすというゲノムを宿主細胞に組み込む侵入者ですが、この性質をうまく利用したのがウイルスベクターです。
レトロウイルスからウイルスになる遺伝子を取り出し、治療に使いたい遺伝子を代わりに導入します。治療用遺伝子を持ったレトロウイルスを細胞に導入させると、細胞内でこの遺伝子のDNAが合成され、宿主染色体に組み込まれます。このようにして、治療効果のある細胞を作ることができます。
レトロウイルスベクターのイメージ
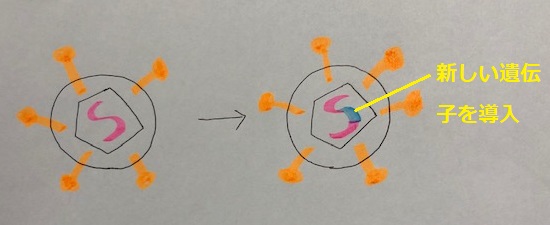

出典:https://cnx.org/contents/ceM19Q1y@3/Gene-Therapy
ウイルスによる遺伝子導入はあのiPS細胞樹立でも応用されていましたね。
2007年にヒトで初めてiPS細胞の樹立に成功したとき、初期化因子であるOct3/4、Sox2、Klf4、c-Mycの導入にはレトロウイルスが使われていました。初期化因子を過剰発現させることで、体細胞の核の記憶をリセット、つまりiPS細胞へと初期化していました。
しかし、外来遺伝子の再活性化により腫瘍が発生するリスクがあるため、レトロウイルスベクターやレンチウイルスベクターなどのウイルスベクターの使用は控えられるようになりました。
ところが、その後、内在性レトロウイルスが初期化促進に関与していることがわかり、役に立たないと思われていたレトロウイルスが脚光を浴びることになりました。
内在性レトロウイルスとは
レトロウイルスが実はすごかった!というお話の前に、内在性レトロウイルスについてみてみます。
レトロウイルスは内在性レトロウイルスと外来性レトロウイルスに分類されます。
ざっくり言うと、
外来性レトロウイルスは、あつあつのフライドポテト(=すぐ食べられる≒すぐ動ける)、
内在性レトロウイルスは、冷凍保存されたフライドポテト(=すぐ食べられない≒眠っている)です。
もう少し丁寧に説明したのがこちら。
外来性レトロウイルス:個体から個体へ感染可能なウイルス
内在性レトロウイルス:過去に感染した外来性レトロウイルスが生殖細胞に入り込み、宿主細胞のゲノムの一部になったもの
ヒトのゲノムは10億塩基対もの長さのDNAからなりますが、実際に使われている情報量は全体のごく一部です。残りの大部分は、不要な塩基配列で占められています。その不要な配列の中に、内在性レトロウイルスが含まれています。
外からやってきたレトロウイルスが生殖細胞や発生初期の細胞に組み込まれると、ウイルス遺伝子の転写が抑制され、内在化して、ゲノムが次の代へと受け継がれます。
自分のものだと思っていた身体には、他の生物の遺伝子が寄生しているというわけですね。私たちの身体は、ウイルスに感染したコンピュータといってもいいかもしれません。
【異種移植に希望】内在性レトロウイルスを不活性化した「無毒ブタ」の誕生
内在性レトロウイルスは、活性化が抑えられた状態でゲノムに潜んでいるものです。
もしこのウイルスが活性化し、動き回るようになると、ゲノムに入り込んで突然変異を引き起こしかねません。
この問題が特に懸念されるのが、異種移植です。
例えば、ブタの臓器は大きさや機能面でヒトに近く、ドナー臓器不足を解決しうる有効な供給元となりえますが、ブタに潜む内在性レトロウイルスは移植において懸念事項となります。
そのため、内在性レトロウイルスが不活性化されたブタの研究が行われてきました。
2017年8月に米国と中国の研究者が、内在性レトロウイルスを不活性化したブタを誕生させることに成功しました。これは世界初の「無毒」のブタとして注目を浴びました。
ちなみに、この研究の中心人物であるヤン・ルハン氏はこんなに若い女性です。

出典:百度百科
では、先ほどのiPS細胞樹立において、厄介者だったレトロウイルスが実はすごかったというお話に戻ります。
【iPS細胞】初期化・分化の鍵となる内在性レトロウイルスの働き
山中伸弥先生と高橋和利先生は、iPS細胞を他の細胞に分化させようとしても、分化能の低いiPS細胞(分化抵抗性iPS細胞)が存在する原因を研究し、その仕組みを解明しました。
この研究の主役が、内在性レトロウイルスの一種であるHERV-Hです。
わかったポイントは次の2点。
ポイント① 内在性レトロウイルスの一種であるHERV-Hの活性化が初期化を促進する。
ポイント② iPS細胞の分化抵抗性の原因は、Klf4の異常発現によるHERV-Hの活性化である
これではよくわからないと思いますので、図解で説明します。
ポイント① HERV-Hの活性化が初期化を促進する
初期化の途中でHERV-Hの発現量を調べてみると、HERV-Hの発現が一過性に発現していました。この時、HERV-H配列の両端にある反復配列LTR7が活性化されていました。

出典:初期化および分化において鍵となるヒト内在性レトロウイルスの働き

↑初期化途中の時点。
次に、初期化の時にLTR7の活性を抑えてみると、iPS細胞の作製効率が大幅に低下しました。
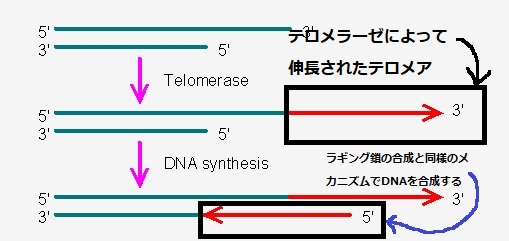
これより、HERV-Hが一過性に活性化することが、初期化を促進していることがわかりました。
つまり、内在性レトロウイルスが初期化を促進していたということです。
ポイント② iPS細胞の分化抵抗性の原因は、Klf4の異常発現によるHERV-Hの活性化である
iPS細胞の初期化因子には、Oct3/4、Sox2、Klf4、c-Mycがありました。このうち、分化能の低いiPS細胞ではKlf4の発現が高くなっていることがわかりました。
そこで、Klf4とLTRの働きをそれぞれ抑えてみたところ・・・
HREV-Hの発現が抑制され、iPS細胞の分化能が通常のiPS細胞と同程度に上がりました。

これより、Klf4の異常な活性 → HREV-Hを活性化 → iPS細胞分化能低下となっていることがわかりました。

ポイント①と②は矛盾するように思えますが、次のように考えました。
初期化のためにはHERV-Hの一過性の活性化が必要だが、HERV-Hが活性化されすぎると逆に分化能が低下してしまうので、HERV-Hの活性は適度に抑制する必要があり、そのためにKlf4の活性を抑える必要がある、ということだと思います。
まとめ
今回はレトロウイルスをめぐるお話を紹介しました。
遺伝子治療から臓器移植、再生医療と幅広く登場するウイルスですね。無毒ブタや内在性レトロウイルスがiPS細胞の初期化を促進しているあたりはとても興味深かったです。
今回お話したのは、レトロウイルスをめぐる壮大な物語のごく一部。他のお話はまた改めてすることにしましょう。
※アイキャッチ画像の出典:http://www.ox.ac.uk
【参考】
異種移植とブタ内在性レトロウイルス:異種移植の経験のある人での追跡研究の報告
ゲノム編集技術により誕生した世界初の内在性レトロウイルスを不活性化したブタ
初期化および分化において鍵となるヒト内在性レトロウイルスの働き
こちらの記事もおすすめ