自分の子どもを抱っこできない女性にとって、3Dプリンタ製人工骨は希望になるのか?

目次
「子どもは1歳になった。しかし、私はまだ子どもを抱くことができない」
2回の妊娠・出産によって、骨密度が大きく低下してしまった女性がいます。
骨の異常に気付いたのは、2回目の出産後。病院で検査すると、骨密度が劇的に低下していることが判明。
生まれたばかりの赤ちゃんを抱っこすることも禁じられ、倒れた自転車を自分で起こすことができなくなるほど、骨密度が低下してしまいました。この疾患は何千万人に1人という確率のようです。
薬物治療を続けても、1年で上昇した骨密度はごくわずか。
彼女は今、仕事復帰を控え、2人の子供の保育園送迎をどうしたらいいのか、悩んでいます。
とても他人事には思えず、人工骨で解決できないだろうかと考えてみました。
すると、3Dプリンタで造形した人工骨が既に販売されていること、移植後に骨に転換される人工骨の存在を知りました。
そこで、今回は3Dプリンタで「骨をつくる」技術をご紹介します。
骨移植の種類
骨は再生能力の高い組織です。通常の骨折では、骨折部分を固定することで自然に骨が癒合します。
一方で、先天的な骨欠損、大きな外傷による骨折などでは骨欠損が大きく、自然な骨癒合では治療できないことがあります。その場合にとられる措置が骨移植です。
骨移植は次の種類があります。
自家骨移植
他家骨移植
異種骨移植
人工骨移植
日本では自分の骨を摘出し、移植する自家骨移植が中心になっています。
欧米では、手術で廃棄される骨や死体から提供される骨を移植する他家骨移植が中心です。
異種骨移植は、ウシやブタなど移植を受ける側と異なる生物種から採取した骨を移植することを指します。
人工骨移植は、人工的に合成されたバイオマテリアルを移植するものです。
自家骨移植のメリット・デメリット
メリット
・自分の生きた骨を移植するため、骨形成能が備わっているだけでなく、強度など力学的特性も必要なものに近い
デメリット
・自分の骨の一部を採取する必要があるため、大きさ、形状に制限がある
・欠損部分に短期間で加工するのが大変
・手術が長時間にわたるため感染症のリスクが高まる
一方、他家移植はどうでしょうか?
他家骨移植のメリット・デメリット
メリット
・自身の摘出手術が不要
デメリット
・倫理的問題がある
・献体からの感染の問題がある
それぞれの移植にはメリット、デメリットがありますので、解決手段として人工骨の開発研究がおこなわれてきました。
人工骨が求められる背景
自家骨移植と他家骨移植に共通する問題はなんでしょうか?
必要なときに必要な量が手に入らない可能性があることです。
欠損部分が大きい場合、自家骨移植では必要な骨を提供できない可能性があります。他家骨の場合、他人の骨を移植するため大きさはカバーできるかもしれません。しかし、常に入手できるとは限りません。
また、両者いずれの場合にも、手術が始まってから位置を合わせ、骨を必要な形に削り、もし合わない場合は再度削る、という作業が求められます。このため手術時間が長くなり、患者の負担が大きくなります。
すると、人工骨には次のような特徴が求められると考えられます。
①必要な時に作れる
②必要な量を使える
③すぐに使える形で移植できる
④いずれ体内の骨と同化できる
これまでの自家骨移植と他家骨移植では、①~③の条件を確実に実現することはできません。
従来の人工骨は、リン酸カルシウムを主成分とするハイドロキシアパタイトを高温で焼き固めたブロックや顆粒状のものでした。つまり焼結プロセスが必要でした。
さらに、移植時に医師が移植部位に応じて形を整える必要がありました。焼結しているため手術後に移植部位の骨に置換されず、体内に人工物として残り続けるものでした。
つまり、必要な量を確保できても、焼結が必要で、手術時に成形も必要なため、すぐに使えないという問題点がありました。
また、成長の早い子どもへの移植には適さないという問題がありました。
人工骨の種類
ここでまず、人工骨の種類についてみてみましょう。大きく分けて次の2つになります。
非吸収性の人工骨:ハイドロキシアパタイト
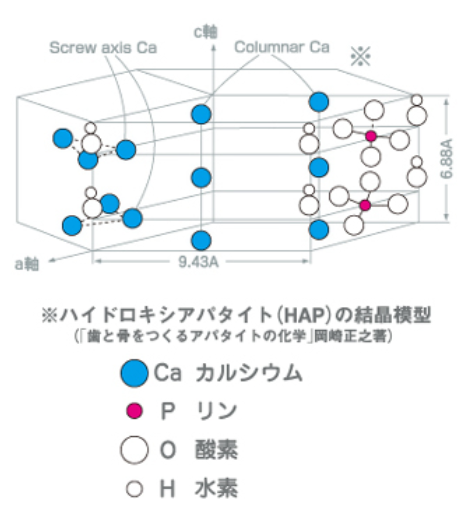
出典:https://www.sangi-co.com/sp/apatite/index.html
骨の無機成分の主成分であるハイドロキシアパタイトというセラミックスを使った人工骨です。
ハイドロキシアパタイトは、骨と異物反応を生じずに骨と強固に結合します。生体骨のように吸収はされまずが、吸収速度は非常にゆっくりで、半永久的に生体内に残存します。実質的に非吸収性の成分です。
吸収性の人工骨:α-TCP、β-TCP
出典:https://knowledge.ulprospector.com/297/tricalcium-phosphate-food-formulations/
ハイドロキシアパタイトが残存型であるのに対し、αリン酸三カルシウム(α-TCP)、βリン酸三カルシウム(β-TCP)は、体内で徐々に分解、吸収され、骨に置換するセラミックスです。
つまり、ハイドロキシアパタイトとリン酸三カルシウム(α-TCP、β-TCP)には次のような違いがあります。
ハイドロキシアパタイト:生体内で吸収されず、異物として半永久的に残存する。
リン酸三カルシウム(α-TCP、β-TCP):生体内で吸収され、骨置換される。
セラミックスの「高硬度」と「脆性」という特性
ここで、セラミックスの特性について考えてみます。
セラミックスは高い強度を示し、融点が高いため耐熱性に優れていますが、脆性を示すという欠点があります。
セラミックスが高強度なのはなぜ?
それは、金属と異なり、セラミックスは共有結合、イオン結合を主とするためです。
結合の強さは、共有結合、イオン結合の方が金属結合より強いため、金属に比べて強度が高く、高温まで溶融しないのです。
では、セラミックスの欠点である「脆性」とは何でしょうか?
脆性とは、破壊しやすい性質を示しています。
金属は一部に欠陥が発生しても、臨機応変に状態を変えて自身が崩れないようにキープすることができます。セラミックスは金属のような臨機応変さに欠け、もろくて割れやすいのです。
金属が成績はそれほど良くないけど、打たれ強いのに対し、セラミックは学歴がとても高いけど、ちょっとの挫折で立ち直れなくなってしまうガラスのハートの持ち主、という感じでしょうか。

先ほどの人工骨の種類に戻ると、
ハイドロキシアパタイトは非吸収性、リン酸三カルシウムは吸収性でした。
セラミックスが破壊しやすい性質を持つことを考えると、体内に半永久的にハイドロキシアパタイトからなる人工骨がある場合、「脆性破壊」という問題を抱えて使用することになります。それでは問題があるため、ハイドロキシアパタイトの人工骨を作る場合、脆性破壊に対する材料設計が必要になります。
一方で、リン酸三カルシウムの人工骨は、体内に移植後、時間の経過とともに分解、吸収されて骨置換します。つまり、最終的に骨に置換するリン酸三カルシウムを使用する場合、「脆性破壊」という課題を克服できることになります。
当初はハイドロキシアパタイトを使った人工骨が開発されていました。近年では、吸収性のリン酸三カルシウムを使った人工骨や、複合材料を使った人工骨が開発されています。
ここで、理想的な人工骨に求められる(私の考える)特性をもう一度見てみましょう。
①必要な時に作れる
②必要な量を使える
③すぐに使える形で移植できる
④いずれ体内の骨と同化できる
リン酸三カルシウムを使うと、①②④は解決できますね。
では、③の「すぐに使える」はどのように実現するのでしょうか?
3Dプリンタを使って骨を「作る」
ここでようやく3Dプリンタの登場です。
3Dプリンタを使うことで③も解決できるようになりました(後述)。
従来の人工骨は、ある大きさのセラミックスを必要な形に削って成形する必要がありました。つまり、彫刻ですね。

3Dプリンタを使うと、必要なところに必要なだけ材料を吐出すればよいですよね。これは、粘土に似ています。

これは、印刷技術が版画→インクジェットへと変遷してきたのにも似ていませんか?


印刷技術の歴史が、
木に彫刻を施して印刷していた版画から、
望む場所に微細なインクを吹き付けて印刷するインクジェットへと変わったのと同様に、
人工骨も、
削らなければ完成できなかったものから、
3Dプリンタを使うことで、個人にあった人工骨を作り、すぐに使えるようになりました。
まさに人工骨もテーラーメイドが可能になりつつあるということです。
リコーの人工骨
今回はリコーの、リン酸三カルシウムを主成分として、3Dプリンタを活用した人工骨をご紹介します。
これは、2018年4月4日に発表された理化学研究所との共同研究の成果を報告したものです。
リコーの人工骨は、インクジェット方式を利用した3Dプリンタで製造しています。
インクジェット方式は、バインダージェット方式ともいい、一面に敷いた粉末層に、結合剤となる凝固インクを塗布し、粉末を硬化させることで造形物を得る方法です。
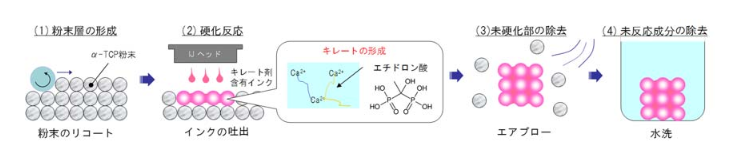
出典:あなたの骨を作ります -高い強度と骨置換性を持つ人工骨を3Dプリンターで製作する-
つまり、私たちが普段使うインクジェットの「紙」を「粉末層」に変え、「インク」を「結合剤」に変えたイメージですね。
リコーの技術では、一面に敷いたリン酸三カルシウム(α-TCP、β-TCPなど)の粉末層にエチドロン酸が吐出されます。すると、エチドロン酸がリン酸三カルシウムのCaを補足し、キレート反応により硬化します。このようにして、エチドロン酸(凝固インク)が塗布された部分は数秒で硬化します。強度は自家骨と同等レベルの強度25~30MPaとされています。
また、従来と異なり、造形物は焼成する必要がなく、数分間水洗いすればすぐに使うことができます。
以下の写真より、移植後に体内の骨組織に入れ替わっていることがわかります。
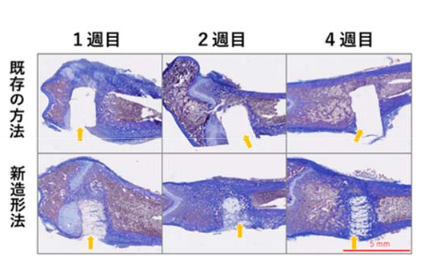
出典:あなたの骨を作ります -高い強度と骨置換性を持つ人工骨を3Dプリンターで製作する-
リコーの「人工骨」に関する関連特許
上記発表内容の特許はまだでていないようですので、リコーの関連する特許を読んでみました。
特開2015-187058
【発明の名称】粉末積層造形用硬化液、積層造形セット及び積層造形物の製造方法
【発明者】渡邉政樹
特開2015-187058では、上述したハイドロキシアパタイトの残存性に関する懸念が触れられています。
つまり、ハイドロキシアパタイトが体内に残存することで不具合を生じる可能性を回避するために、生体内で分解、吸収されるリン酸三カルシウムを使っています。具体的にどのような不具合かは触れられていませんが、脆性破壊や異物として残るリスクだと考えられます。
これまでの人工骨ではハイドロキシアパタイトも使われてきたことは上述の通りですが、脆性破壊を回避するための材料設計や、異物として半永久的に残存することなどから、現在はリン酸三カルシウムや複合材料を使った人工骨開発が主流なのだと思います。
リン酸三カルシウム(TCP)には、低温で安定なα-TCPと高温で安定なβ-TCPがあります。α-TCPの水への溶解度は、β-TCPよりも大きく、加水分解反応によりハイドロキシアパタイトに転移します。
リコーの特許のポイントは、ハイドロキシアパタイトへの転移を避けることでした。
上述した通り、TCPは体内で骨置換されますが、ハイドロキシアパタイトは骨置換されません。ハイドロキシアパタイトが体内に残存することで不具合を生じる可能性を回避するために、ハイドロキシアパタイトへの転移を避けたいのだと思います。
そのため、エチドロン酸やフィチン酸といった分子内にリン酸基を有するキレート剤を使って、TCPのカルシウムイオンを捕獲し、生体内に入れた時にハイドロキシアパタイトに転移するのを防止しています。こうすることで、生体に移植後も、体内で分解され、骨に置換されるTCPのままでいることが可能となり、長期にわたる副作用の心配が減るのではないかと思います。
つまり、リコーの特許でエチドロン酸やフィチン酸は、TCPがハイドロキシアパタイトに転移するのを防ぐ役割と、粉末層に吐出された際に粉末層を硬化させる役割の、2つの役割を担っていると考えられます。
ちなみに、特開2015-187058では焼結工程が含まれていますが、先に触れた2018年4月4日のリコーの発表では焼結不要とされています。
どのような技術改良がおこなわれたのか興味がありますね。
NEXT21の人工骨(CT-Bone)はすでに上市済み
国内ではリコー・理化学研究所の研究のほか、NEXT21(ネクスト21)が同じく理化学研究所、そして東大などと開発した人工骨(CT-Bone)が既に製造販売承認を受け、昨年より販売が開始されています。NEXT21の人工骨についても、改めてご紹介する予定です。
冒頭で書いた女性にとって、根本的な解決方法になる技術革新が起きることを祈るばかりです。
関連記事
バイオプリンティングの原理、各方式のメリット・デメリットを解説
バイオプリンタで患者の細胞から血管付き人工心臓の作製に成功【原理を解説】(テルアビブ大学)
3Dプリンタが実現するドラッグデリバリーシステム -胃内滞留デバイスー
参考:
あなたの骨を作ります -高い強度と骨置換性を持つ人工骨を3Dプリンターで製作する-
「加工材料の知識がやさしくわかる本」西村仁
「機械材料学」 日本機械学会
「化学便覧」 応用科学編Ⅰ
「再生医療のためのバイオマテリアル」田畑泰彦
人工臓器学会誌2014年43巻3号「人工骨」
人工臓器学会誌2011年40巻1号「人工骨の歴史と最新デザインコンセプト」
材料学会学会誌2014 年 63 巻 7 号 p. 563-568初学者のためのバイオマテリアル